Aerobe glycolyse (katabolisme)
Aerobe glycolyse (katabolisme)
Laatste bijwerking : 2021.11.19
De eerste stap in het katabolisme van suikers (gluciden) is de decompositie van macromoleculen in enkelvoudige suikers. Deze decompositie heeft plaats in de dunne darm. Organische moleculen worden op deze wijze omgezet in voor het organisme bruikbare elementen. De kleine moleculen kunnen door de darmwand heen naar de bloedbaan en uiteindelijk in de cel.
-
-
koolhydraten uit de voeding worden initieel omgezet in enkelvoudige suikers (glucose) en vervolgens opgenomen in het bloed.
-
dit veroorzaakt een stijging van de glykemie, waarop als antwoord de insulinesecretie wordt gestimuleerd.
-
hierbij wordt het circulerend glucose geabsorbeerd uit de bloedbaan naar de lever en de weefsels (= cellen).
-
hierna daalt de glykemie terug en wordt het overtollige insuline afgebroken in de lever.
-
De afbraak van glucose tot koolstofdioxide (CO2) en water wordt suikermetabolisme of koolhydraatmetabolisme genoemd. Dit proces bestaat uit 4 stappen : glycolyse, oxidatieve decarboxylering, citroenzuurcyclus, respiratieketen en oxidatieve fosforylering.
-
-
45% van alle opgenomen suikers uit de voeding gaat naar de hersenen en slechts 10% naar de spieren. De rest dient om alle biochemische processen in stand te houden.
-
-
-
20% van alle zuurstof in het lichaam dient om energie te genereren.
-
Overzicht inhoud :
 Aerobe of anaerobe glycolyse
Aerobe of anaerobe glycolyse
 Overzicht verdere pathways
Overzicht verdere pathways
 Oxidatieve decarboxylering
Oxidatieve decarboxylering
 Citroenzuurcyclus
Citroenzuurcyclus
 Respiratieketen
Respiratieketen
 Oxidatieve fosforylatie
Oxidatieve fosforylatie
 Praktisch
Praktisch
 Schematisch
Schematisch
Inhoud :
 Aerobe of anaerobe glycolyse :
Aerobe of anaerobe glycolyse :
-
-
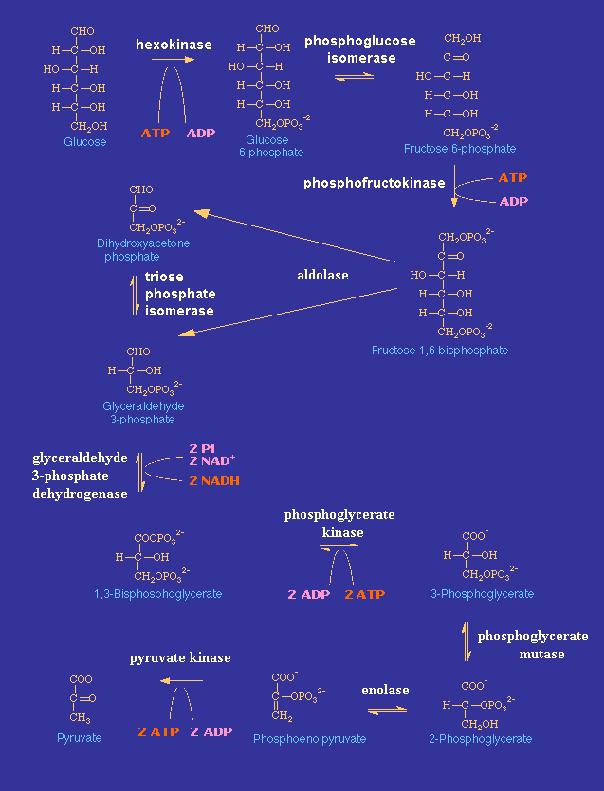
De glycolyse start in het cytoplasma. Hierbij wordt 1 molecule glucose afgebroken tot 2 moleculen pyrodruivenzuur.
-
C6H12O6 + 2 ADP + 2 Pi + 2 NAD+ ---> 2 C3H4O3 + 2 ATP + 2 NADH + 2 H+ + 2 H2O
of
1 x glucose ----> 2 pyrodruivenzuur
Doch allereerst dient energie (ATP) geïnvesteerd worden om het suikermolecule in een geactiveerde toestand te brengen, die zich leent voor de splitsing in 2 x triose-fosfaat.
-
-
-
glucose ---> via hexokinase + ATP ---> glucose 6-fosfaat ---> fructose 6-fosfaat
-
-
-
-
-
-
fructose 6-fosfaat ---> via fosfofructokinase (PFK) + ATP ---> fructose 1.6-fosfaat ---> splitsing in 2 x glyceraldehyde 3-P
-
-
-
-
-
-
-
-
de 2 glyceraldelyde 3-fosfaat moleculen vormen zich om in 2 pyruvaatmoleculen.
-
-
-
-
![]() De geïnvesteerde energie wordt achteraf teruggewonnen bij de oxidatieve overgang van triosefosfaat naar fosfoglycerolzuur, waarbij H+ wordt afgegeven aan het coënzym NAD+ voor de vorming van NADH.
De geïnvesteerde energie wordt achteraf teruggewonnen bij de oxidatieve overgang van triosefosfaat naar fosfoglycerolzuur, waarbij H+ wordt afgegeven aan het coënzym NAD+ voor de vorming van NADH.
NAD+ + H+ + 2e- ---> NADH
Bij de omzetting van fosfoglycerolzuur in pyodruivenzuur wordt een nettowinst van ATP verkregen. Voor elke molecule glucose, 2 moleculen ATP worden verbruikt doch 4 moleculen ATP worden terug gewonnen. De winst bedraagt dus 2 x ATP.
-
-
Afhankelijk van de nood van het organisme wordt dit pyrodruivenzuur verder omgezet :
-
-
-
-
in CO2, water en ATP (aerobe glycolyse via de citroenzuurcyclus in de mitochondriën : = decarboxylatie via het pyruvaat dehydrogenase enzymcomplex in CO2, NADH en acetylCoA ) : TAMELIJK TRAAG PROCES.
-
-
OF in
-
-
-
in melkzuur en ATP (via de anaerobe glycolyse in het cytoplasma) : REDELIJK SNEL PROCES.
-
-
Iedere weg laat de regeneratie toe van NADH in NAD+. Dankzij de regeneratie van NAD+ kan de glycolyse in afwezigheid van zuurstof toch doorgaan.
De metabole snelheid tussen de aerobe en de anaerobe glycolyse is verschillend : de enzymactiviteit in de mitochondria is langer dan deze in het cytoplasma, waardoor bij overaanbod van glucose meer lactaat (aanzuring!) en minder ATP door oxidatieve fosforylatie, wat leidt tot gevoelens van energietekort en moeheid.
---> vervolgens, dreigt hier ook, door de snelle glucose verbranding, een hypoglykemie, wat op zijn beurt een reactie uitlokt met activatie en vrijstelling van
-
-
-
-
glucocorticoïden, adrenaline en cortisol in de bijnier
-
glucagon uit de alfacellen in de pancreas
-
-
-
Hierdoor :
-
-
-
-
-
ontstaan van hypoglykemie-toestand
-
ontstaan van hypoadrenia-toestand (uitputten van de bijnier)
-
het glycogeen in de lever en in de spiercel pogen het glucose in het bloed aan te vullen, de patiënt hunkert naar suiker, meestal als geraffineerde voeding, waardoor de nutriënten tekorten niet worden of kunnen aangevuld worden
-
de voortdurende overmaat lactaat zal een permanente bijnierstimulans veroorzaken en een chronische stress situatie onderhouden, door het creëren van een constante weefselacidose (lactaatacidose)
-
-
-
-
![]() Risico op chronische stress-situatie door de constante overmaat lactaat (acidose! zie Gluconeogenese).
Risico op chronische stress-situatie door de constante overmaat lactaat (acidose! zie Gluconeogenese).
Opgelet :
-
-
-
-
-
-
de lactaatproductie regelt eveneens de zuurgraad (pH) van de weefsels bij de vorming van nieuw weefsel, bij groei, bij regeneratie en herstel van weefsels, bij afgifte van zuurstof in de weefselcellen (Bohr-effect).
-
-
-
-
-
Noot:
Deze productie van ATP uit lactaat bij de anaerobe omzetting van glucose is wel de enige energiewinningsmogelijkheid van erytrocyten, daar rode bloedcellen geen mitochondriën bezitten. Het toxische lactaat wordt verwijderd tijdens de gluconeogenese.
 Overzicht verdere pathways :
Overzicht verdere pathways :
Ook via het glucose 6-fosfaat uit de glycolyse :
-
-
---> via het 5-G6P dehydrogenase ---> ribose 5-fosfaat ---> nucleotiden (pentose phosphate pathway = PPP)
-
-
-
---> oxydatie met NAD+ ---> inositol 1 fosfaat ---> + fosfatydyl ---> Fosfatidyl-Inositol (PI) (---> Fosfo-inoside-cascade systeem)
-
-
-
---> UDP-glucose ---> oxidatie via het UDP-glucose dehydrogenase ---> glucuronzuur ---> in de ontgifting.
-
-
-
---> UDP-glucose ---> UDP-galactose ---> nodig voor inbouw in sfingolipiden.
-
-
-
---> fructose 6-fosfaat ---> via D glucosamine-P isomerase, Gln ---> D-glucosamine 6-P ---> glucosamine ---> + proteïne ---> proteoglycanen.
-
-
-
---> fructose 6-fosfaat ---> glucosamine ---> via AcCoA/B5 (Krebs) ---> N-acetylneuraminezuur (NANA, siaalzuur) ---> CMP-siaalzuur ---> glycoproteïnen ---> proteoglycanen.
-
-
-
---> fructose 6-fosfaat ---> 1.3 difosfaat glyceride ---> 2.3 Difosfo-Glyceraat (2.3 DPG) (zijtak bij extra vraag : speelt een rol in de O2 opname/afgifte van Hb : zie Bohr-effect).
-
-
-
---> fructose 6-fosfaat ---> DHAP (dihydroxyacetonfosfaat). Deze laatste dient als substraat voor de gluconeogenese of wordt via fructolyse omgezet in lactaat.
-
 Het organisme bepaalt zelf het evenwicht tussen proteoglycanen en glycoproteïnen.
Het organisme bepaalt zelf het evenwicht tussen proteoglycanen en glycoproteïnen.
 Oxidatieve decarboxylering :
Oxidatieve decarboxylering :
In de glycolyse wordt glucose omgezet tot pyrodruivenzuur. Voor het binnentreden in de citroenzuurcyclus wordt het acetylgedeelte (CH3CO) van acetylCoA (verkregen uit pyroduivenzuur via decarboxylatie en oxidatie (samen : oxidatieve decarboxylatie)) gevormd, reactie gekatalyseerd door het enzymcomplex PDH (pyruvaat dehydrogenase).
De oxidatieve decarboxylering is dus de tweede stap in het koolhydraatmetabolisme :
Vindt na diffusie doorheen de membraan in het mitochondrion plaats : onder aerobe omstandigheden wordt pyroduivenzuur oxidatief (door oxidatieve decarboxylering) onomkeerbaar omgezet in geactiveerd azijnzuur. Hierbij speelt het coënzym A de rol van dragermolecule bij de vorming van het enzymcomplex Acetyl-Coënzym A.
C3H4O3 (pyruvaat) - CO2 + CoA-SH ---> - 1 Koolstof ---> AcetylCoA (= C2)
(De term decarboxylering beschrijft een reactie waarbij een carboxylgroep een carbonzuur (R-COOH) verlaat in de vorm van CO2)
(azijnzuur, ook het actieve product van appelazijn, verbetert de insulinegevoeligheid en vermindert de vetvorming door het lichaam te helpen glucose efficiënter te verbranden en minder vet op te slaan na de maaltijd)
Enzymcomplex PDH
Het Pyruvaat Dehydrogenase complex (PDH) omvat meerdere enzymen en vereist 5 verschillende coënzymen : CoA (---> vit B5), TPP (thiamine pyrofosfaat ---> vit B1), liponzuur, FAD (---> vit B2) en NAD+(---> vit B3).
Het netto resultaat van de reactie in het PDH complex :
Pyruvaat + CoA + NAD+ ---> CO2 + AcCoA + NADH + H+
-
-
-
TPP neemt de acetylgroep van pyruvaat op, geeft hem af aan liponzuur en verder aan het CoA-SH.
-
-
-
-
-
De activiteit van het PDH complex wordt geregeld door de staat van fosforylering. Het is bekend dat Ca2+ en Mg2+ het PDH fosfatase activeren.
-
-
-
-
-
In vetweefsel laat insuline de activiteit van PDH toenemen en in hartspieren laten catecholaminen (adrenaline, noradrenaline...) de activiteit van PDH toenemen.
-
-
-
-
-
Roken, kwik (vis, tandamalgaam....), arseen : blokkeren het dehydrogenase enzym.
-
-
-
-
-
Het gevormde NADH zal terug geoxideerd worden binnen de respiratieketen en laat zo de synthese toe van 3 ATP.
-
-
1 x glucose ---> 2 pyruvaat ---> 2 acetylCoA ---> 2 x NADH ---> 2 x 3 ATP = 6 ATP
![]() De grootste hoeveelheid ATP die de cellen nodig hebben om de homeostase te onderhouden, wordt geproduceerd door de oxidatie van pyruvaat in de citroenzuurcyclus. Het gevolg van een PDH complex deficiëntie is dus een tekort aan energie in het CZS.
De grootste hoeveelheid ATP die de cellen nodig hebben om de homeostase te onderhouden, wordt geproduceerd door de oxidatie van pyruvaat in de citroenzuurcyclus. Het gevolg van een PDH complex deficiëntie is dus een tekort aan energie in het CZS.
Opgelet :
-
-
De omzetting van pyrodruivenzuur ---> acetaat is een onomkeerbaar proces! Eenmaal omgezet kan acetaat niet meer gebruikt worden om pyruvaat te synthetiseren. Pyruvaat kan alleen worden verkregen uit afbraak van grotere biomoleculen.
-
![]() De cel moet op dit punt dus beslissen :
De cel moet op dit punt dus beslissen :
-
-
-
ofwel dat het pyruvaat uit de glycolyse wordt gebruikt om energie te produceren,
-
ofwel voor andere biosynthetische reacties (Anaerobe glycolyse en verder gluconeogenese, vetzuursynthese in citraat-pyruvaat cyclus...).
-
-
Het enzymcomplex PDH staat op dit kruispunt en controleert de flux van pyruvaat naar de verschillende mogelijke metabole polen.
-
-
Een deficiëntie in dit enzymcomplex beperkt de productie van citroenzuur. De citroenzuurcyclus (Krebs) stopt dan!! De grootste hoeveelheid energie (ATP) voor de cellen wordt echter geleverd door de oxidatie van pyruvaat in de citroenzuurcyclus: dus bij PDH deficiëntie ---> tekort aan energie.
-
-
-
Het overschot aan pyruvaat, onstaan bij deze deficiëntie, wordt omgezet in lactaat (melkzuur) en er ontstaat een zuurvergiftiging (acidose) in het bloed (lactaatacidose).
-
 Citroenzuurcyclus
Citroenzuurcyclus
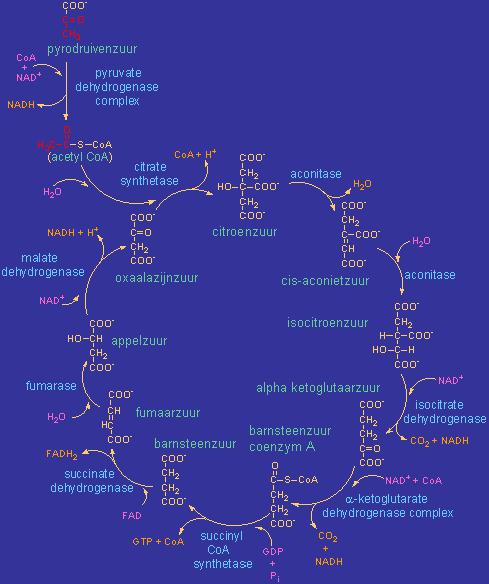
of Krebscyclus (naar de ontdekker), of TCA-cyclus (naar de 3 COOH-groepen van citroenzuur) :
De citroenzuurcyclus is een belangrijke draaischijf in het metabolisme van suikers, eiwitten en vetten.
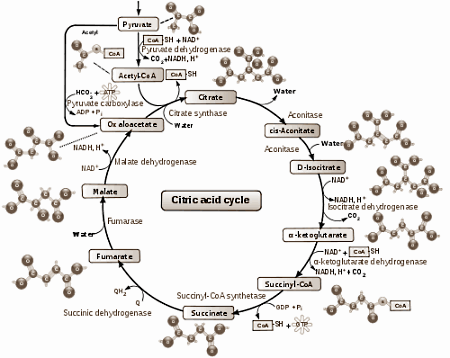
Vindt plaats in de mitochondria en vereist de aanwezigheid van zuurstof (ademhaling, belang van oxygenatie van de weefsels, goede bloedsomloop voor aanvoer, voldoende rode bloedcellen voor het transport...)...
De citroenzuurcyclus bestaat uit een serie chemische reacties die essentieel zijn voor de oxidatieve stofwisseling van glucose en andere eenvoudige suikers. Het doel van deze cyclus is de vorming van NADH en FADH2 voor de respiratie- of ademhalingsketen.
De citroenzuurcyclus is een oxidatiecyclus (oxidatie is het proces waarbij elektronen worden afgegeven) waarbij brandstofmoleculen uit vetten, suikers en AZ geoxideerd worden tot koolstofdioxide (CO2), het eindproduct van de citroenzuurcyclus. Eigenlijk worden deze moleculen niet zelf geoxideerd maar is zuurstof nodig voor de heroxidatie (regeneratie) van de gereduceerde coënzymen (in de glycolyse), NADH en FADH2, wat gepaard gaat met elektronen-overdracht via een carriermechanisme waarbij zuurstof de uiteindelijke elektronenacceptor is.
Resultaat : Suiker ----> CO2 en H+ en verder NAD+ + H+ + 2e- ---> NADH
-
-
-
iedere cyclus produceert 3 NADH moleculen (uit NAD+) en 1 x FADH2 (uit FAD) : zie verder "Respiratieketen",
-
één zo'n cyclus levert 1 molecule GTP (uit GDP) (geen ATP!). Verder via de respiratieketen en de oxidatieve fosforilatie, wordt 1 molecule ATP geleverd (gevormd bij het vrijkomen van 4 elektronen).
-
-
Voor elke glucose molecule ---> 2 pyruvaat ---> 2 rondjes in de citroenzuurcyclus ---> 2 x GTP (ATP).
De in de cyclus voorkomende tussenproducten dienen als grondstof voor de biosynthese van nieuw celmateriaal.
Zie ook : "Citroenzuurcyclus" - "Externe beïnvloeding" - "Interne beïnvloeding".
 Respiratieketen (ademhalingsketen) :
Respiratieketen (ademhalingsketen) :
Bij normale cellulaire ademhaling worden elektronen afkomstig van het voedsel dat we consumeren door een reeks eiwitcomplexen in de mitochondriën geleid. Dit proces, bekend als de elektronentransportketen, leidt uiteindelijk tot de productie van ATP, de energievaluta van de cel. Zuurstof dient als de laatste elektronenacceptor in deze keten.
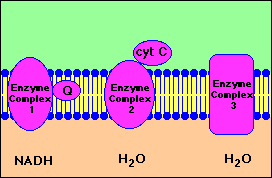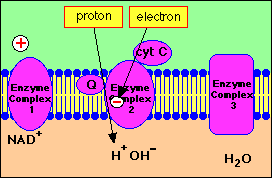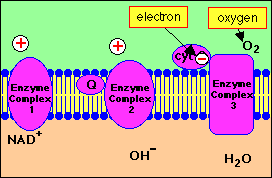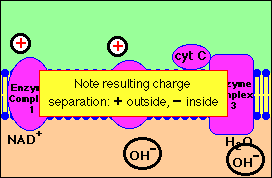
De overdracht van elektronen van het substraat op zuurstof heeft niet rechtstreeks plaats maar verloopt via een vaste serie reacties die bekend staan als de elektronentransportketen of respiratieketen. Het speelt zich af in de binnenste membraan van de mitochondriën.
Iedere schakel in de keten reduceert hierbij een volgende schakel en wordt hierbij zelf geoxideerd. Elk kan dus een reversibele redoxreactie ondergaan. Een soort roltrapsysteem dus. Het NAD+/NADH-redoxkoppel is hierin de eerste schakel. Een ander bekend koppel is FAD/FADH2.
De stroom elektronen genereert ook een magnetisch veld binnen je mitochondriën. Dit magnetische veld is belangrijk voor het aantrekken van zuurstof, dat essentieel is voor de energieproductie, en voor het vasthouden van reactieve zuurstofspecies binnen de mitochondriën.
Resultaat : 4H+ + O2 + 4 e- ---> 2 H2O + energie voor omzetting ADP + P ---> ATP + Pi
(P : anorganisch fosfor ; Pi = fosforesters)
Of : C6H12O6 + 6 O2 ---> oxidatie ---> 6 CO2 + H2O + energie
Voor elke glucose molecule ---> 2 pyruvaat ---> 2 rondjes in de citroenzuurcyclus :
De respiratieketen bevat een enzymketen van 4 enzymcomplexen :
-
-
I het NADH dehydrogenase complex (flavoproteïne complex) (vit B3)
-
II het succinaatdehydrogenase complex en FMN (flavoproteïne complex) (vit B2)
-
III het ubiquinondehydrogenase complex met cytochromen b en c1
-
IV het cytochroom oxidase complex (Fe, Cu, ...)
-
Opdat de respiratieketen ten volle haar rol zou kunnen spelen zijn volgende elementen belangrijk :
-
-
ideale EVZ-samenstelling van de mitochondriummembraan
-
voldoende gereduceerd (dus vers) voedsel
-
voldoende zuurstof aanvoer via de celademhaling (bewegen!)
-
voldoende mevalonzuur (cholesterolsynthese) voor aanmaak cytochroom (dus ook voldoende Cu, Fe...)
-
voldoende Q10 synthese (uit cholesterol)
-
voldoende vitamine B3 (precursor voor NAD)
-
detoxificatie : geeft terug een versnelde respiratie en een stijging van de oxidatieve fosforylatie, waardoor de ATP-productie stijgt en de eiwitsynthese versnelt
-
antioxidantia : door versnelde respiratie : opletten voor zuurstoflekken : Vrije Radicalen pathologie
-
 Oxidatieve fosforylatie :
Oxidatieve fosforylatie :
Bij het elektronentransport vindt een geleidelijke verlaging van energie plaats : een deel van de energie wordt opgeslagen in de vorm van ATP uit ADP en fosfaat : de oxidatieve fosforylatie.
De oxidatieve fosforylatie = oxidatie (afstand van elektronen) + fosforylatie (opname van fosfaatgroep).
-
-
De oxidatie neemt plaats in de volgende omkeerbare reactie :
-
NADH + ubiquinon (CoQ10) <=> NAD+ + ubiquinol met CoQ10 en Mg2+ .
Normaal is de interne mitochondriale membraan ondoorlaadbaar voor protonen. Nochtans gedurende de elektronenflux met transfer van protonen ontstaat een protongradient tussen beiden zijden van de membraan, welke de synthese van ATP via het ATP synthase mogelijk maakt. De respiratieketen en de oxidatieve fosforylatie zijn dus gepaard via deze protongradiënt.
-
-
Fosforylatie vindt plaats in de volgende omkeerbare reactie :
-
ADP + fosfaat ---> ATP synthase ---> ATP + H2O
Ook Cu en Fe via de cytochroom oxidase complex b, c en a (chromoproteïnen) komen tussen bij de elektronenoverdracht in de respiratieketen.
De oxidatieve fosforylatie is verantwoordelijk voor de meeste ATP die de cellen nodig hebben als energiebron voor het onderhouden van alle celfuncties.
Noot:
De aanwezigheid van zuurstof is onontbeerlijk : bij zuurstoftekort, kunnen NADH en FADH niet oxideren. Dit houdt in dat er geen energie meer wordt geproduceerd en NAD+ en FAD niet meer geregenereerd worden!
-
-
Wanneer de voorraad NAD+ en FAD uitgeput is zullen de reacties in de citroenzuurcyclus stilvallen omdat deze coënzymen essentieel zijn voor de cyclus. Een tijdelijk tekort kan bv. optreden tijdens perioden van intense inspanning. Wanneer er geen zuurstof voorhanden is kan de citroenzuurcyclus niet plaatsvinden en stapelt het pyrodruivenzuur zich op in de cel. Bij een overmaat pyrodruivenzuur, wordt deze omgezet in melkzuur die een acidose van het bloed veroorzaakt (anaerobe glycolyse).
-
-
bij regelmatige inspanningen, kan het spierweefsel op een niveau functioneren waarbij de citroenzuurcyclus kan blijven bestaan en waarbij melkzuur snel genoeg kan worden afgebroken. In deze situatie, zijn de longen en het bloed in staat de cellen van de spieren van voldoende zuurstof te voorzien, zodat NADH en FADH kunnen worden geoxideerd.
-
-
-
-
Bij vertraging of blokkering van de citroenzuurcyclus, poogt het lichaam dus haar energie (ATP) via de anaerobe glycolyse te betrekken. Hierdoor daalt de bloedglucosespiegel (hypoglykemie...) met als gevolg een hunker naar suiker en activatie van glucagon (pancreas). De overmaat lactaat zal een sterke bijnierstimulans veroorzaken (adrenaline, cortisol vrijmaking). Risico op chronische stress-situatie door de constante overmaat lactaat (acidose : zie "Gluconeogenese").
-
-
De glycolyse ‘verbruikt’ suikers uit de voeding in de cellen door een reeks metabolieten te produceren tijdens het chemische proces waarbij glucose wordt afgebroken. Metabolieten worden onder meer gebruikt om eiwitten te produceren die de cellen nodig hebben. Een van die metabolieten, cyclisch 1,3-fosfoglyceraat, is een heel reactieve verbinding die eiwitten en andere metabolieten kan beschadigen. Alle menselijke cellen en bijna alle levende wezens bezitten dit enzym, met de naam PARK7. Het is in staat om het gevaarlijke cyclische 1,3-fosfoglyceraat te vernietigen. Als PARK7 niet meer actief is, veroorzaakt dit een opeenstapeling van schade in menselijke cellen, maar dat niet alleen. De onderzoekers stelden vast dat hetzelfde verschijnsel zich voordoet in de cellen van muizen en vliegen.
Blijkt dat sommige gevallen van de ziekte van Parkinson te wijten zijn aan de genetische inactivering van PARK7. Blijkbaar kan PARK7 gemakkelijk worden geïnactiveerd door oxidatieve stress van uiteenlopende oorsprong
 .
.
De aerobe glycolyse wordt vooral gebruikt door
de rode trage spiervezels (aerobe spieren) :
-
-
energiebron glucose en vooral vetzuren, via de aerobe glycolyse
-
geschikt voor trage bewegingen
-
vereist meer ijzer (heem) voor de RBC (nodig voor de aanvoer van zuurstof)
-
Na-verbruik
-
 Praktisch :
Praktisch :
Aerobisch bloedprofiel : normaal moet de lactaat/pyruvaat verhouding kleiner zijn dan 1, de verhouding omega6/omega3 kleiner dan 5, de verhouding Fe/Cu ongeveer gelijk aan 1. De voldoende aanwezigheid van carnitine is afhankelijk van vitamine C en lysine, deze van vitamine B12 en B2 is afhankelijk van zijn intrinsiek factor in de maag.
Deficiënt aeroob systeem door :
-
-
-
onvoldoende aeroob spiergebruik, dus te weinig aerobe beweging
-
overgebruik van anaerobe spieren : te kleine of geen loopruimte (vooral bij hokdieren)
-
deficiëntie van essentiële vetzuren : onaangepaste voeding
-
onevenwicht in het vetzuurmetabolisme
-
Cu, Fe, Mn, CoQ10, vitaminen B deficiënties als cofactoren nodig voor het aeroob systeem
-
-
Remming van het aeroob systeem door :
-
-
-
overmaat Cu (koper)... : Cu onderdrukt Fe in de aerobe spieren ; fructose (fruit...) inhibeert de Cu opname
-
aanwezigheid van NaF (natriumfluoride) : verzwakt en verslapt de aerobe spieren
-
melkzuur
-
antibiotica
-
-
 Schematisch :
Schematisch :
|
|
De glycolyse
|
|
|
van glucose
tot
pyrodruivenzuur |
| |
|
|
|
| De citroenzuurcyclus
|
|
|
van pyrodruivenzuur
via het Acetyl Coënzym A
naar citroenzuur
NADH<
met vorming van NADH, FADH2
met vorming van NADH en GTP
|
NADH gaat verder naar de respiratieketen (+ O2) en vervolgens wordt ADP + Pi ---> ATP (oxidatieve fosforilatie)
|
CO2 naar ureumcyclus > NADH
CO2 naar ureumcyclus > NADH
|
|
|
Elektronentransport NADH/NAD
|
|
|
|
|
|